Qu'est-ce que les cannabinoïdes ?
Les cannabinoïdes sont des composés organiques de nature lipidique, capables de moduler un système de signalisation de l'organisme humain : le système endocannabinoïde (SEC). Ce système participe à la régulation de processus tels que la neurotransmission, la réponse immunitaire et l'inflammation, le métabolisme énergétique, la nociception (perception de la douleur) et la réponse au stress.
Le mécanisme d'action des cannabinoïdes repose sur leur capacité à se lier à des récepteurs spécifiques répartis dans différents tissus. Cette interaction peut activer ou inhiber des cascades de signalisation intracellulaire, altérant la libération de neurotransmetteurs, l'expression génique ou la réponse inflammatoire. La spécificité de l'effet dépend à la fois du type de cannabinoïde, du récepteur impliqué et du contexte physiologique dans lequel le signal se produit.
Bien que le terme cannabinoïde soit immédiatement associé au cannabis, sa signification est plus large. Il existe des cannabinoïdes produits par l'organisme lui-même, des composés d'origine végétale et des molécules synthétisées en laboratoire, tous capables de moduler principalement le SEC (et, dans certains cas, d'autres voies de signalisation connexes).
Types de cannabinoïdes et composés modulant le système endocannabinoïde
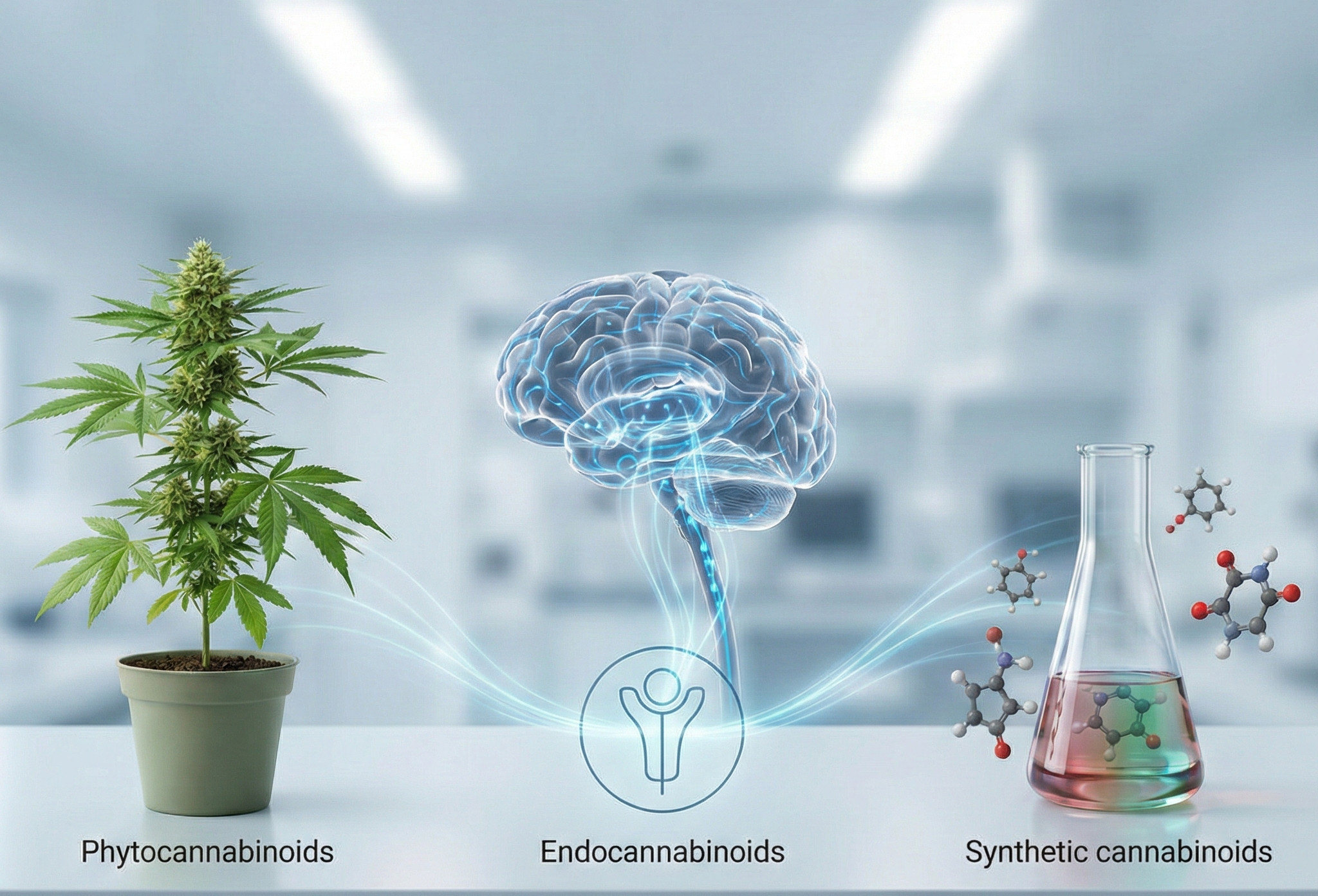 Bien qu'ils interagissent avec les mêmes récepteurs, l'origine de ces composés varie considérablement : de la biosynthèse naturelle dans la plante ou le cerveau, jusqu'à l'origine synthétique.
Bien qu'ils interagissent avec les mêmes récepteurs, l'origine de ces composés varie considérablement : de la biosynthèse naturelle dans la plante ou le cerveau, jusqu'à l'origine synthétique.
Endocannabinoïdes : ceux produits par l'organisme
Les endocannabinoïdes sont des cannabinoïdes synthétisés de manière endogène par le corps humain et d'autres mammifères. Ils ne sont pas stockés en grandes quantités, mais sont produits à la demande à partir de précurseurs lipidiques présents dans les membranes cellulaires.
Les deux principaux endocannabinoïdes caractérisés sont l'anandamide (AEA) et le 2-arachidonoylglycérol (2-AG). Tous deux participent activement à la modulation de la neurotransmission, de la réponse au stress, de l'appétit, de la mémoire et des processus inflammatoires. Contrairement à de nombreux neurotransmetteurs classiques, les endocannabinoïdes agissent de manière rétrograde, régulant la libération d'autres messagers chimiques.
La présence d'endocannabinoïdes a été décrite dans le lait maternel et il a été proposé qu'ils pourraient participer à des comportements précoces comme la succion et à des aspects du développement ; cependant, le détail de ces mécanismes chez l'homme reste un domaine de recherche actif.
Phytocannabinoïdes : ceux d'origine végétale
Les phytocannabinoïdes sont des cannabinoïdes synthétisés par les plantes, Cannabis sativa L. étant l'une des sources les plus riches et diversifiées connues à ce jour. Bien que des composés ayant une activité cannabimimétique aient été identifiés dans d'autres espèces végétales, le cannabis se distingue par la quantité, la variété et la puissance des phytocannabinoïdes qu'il produit.
Pendant des décennies, on a supposé que ces composés étaient exclusifs au cannabis. Bien que l'on sache aujourd'hui que ce n'est pas strictement vrai, cette plante reste la plus pertinente sur le plan pharmacologique et biologique en ce qui concerne le système endocannabinoïde, raison pour laquelle elle constitue le principal foyer d'analyse dans ce domaine.
Cannabinoïdes synthétiques : molécules conçues en laboratoire
Les cannabinoïdes synthétiques sont des composés créés artificiellement dans le but d'interagir avec les récepteurs cannabinoïdes. Certains d'entre eux ont été développés à des fins thérapeutiques, comme le dronabinol, utilisé dans des contextes cliniques spécifiques sous surveillance médicale.
Il faut distinguer les cannabinoïdes synthétiques utilisés comme médicaments (par exemple, le dronabinol dans des contextes cliniques précis) et les mélanges récréatifs de type K2/Spice. Dans ces derniers, la composition est souvent incertaine et certains composés peuvent activer les récepteurs CB1 de manière intense (même en tant qu'agonistes complets), ce qui est associé à un profil d'effets indésirables et de toxicité plus imprévisible que celui du THC.
Cannabinoïdes mimétiques ou cannabimimétiques
Il existe des composés qui, sans appartenir chimiquement à la famille des cannabinoïdes, imitent leur action ou modulent le système endocannabinoïde. On les trouve dans diverses plantes et aliments.
Le bêta-caryophyllène, présent dans le poivre noir, le clou de girofle et le cannabis, est l'un des exemples les plus étudiés pour son affinité sélective pour les récepteurs CB2. D'autres composés présents dans l'échinacée, le cacao ou certaines truffes interagissent également indirectement avec ce système, renforçant son rôle d'interface biochimique entre l'alimentation, l'environnement et la physiologie humaine.
Le système endocannabinoïde (SEC)
Le système endocannabinoïde (SEC) est un réseau régulateur complexe composé de récepteurs cannabinoïdes, d'endocannabinoïdes (messagers lipidiques produits par l'organisme) et d'enzymes responsables de leur synthèse et de leur dégradation. Dans son ensemble, il contribue à l'homéostasie, ajustant de multiples processus physiologiques face aux changements internes ou externes.
Une caractéristique distinctive du SEC est que de nombreux endocannabinoïdes sont synthétisés "à la demande" à partir de lipides membranaires et agissent localement pendant une courte période. Dans le système nerveux, ils peuvent fonctionner comme des signaux rétrogrades : le neurone postsynaptique libère des endocannabinoïdes qui agissent sur les terminaisons présynaptiques, modulant la libération de neurotransmetteurs et la plasticité synaptique.
Les récepteurs CB1 s'expriment principalement dans le système nerveux central, en particulier dans les régions impliquées dans la cognition, la mémoire, le contrôle moteur et la perception de la douleur. Leur activation explique une bonne partie des effets neurologiques du THC, car elle modifie la signalisation synaptique et l'équilibre des circuits neuronaux impliqués dans ces fonctions.
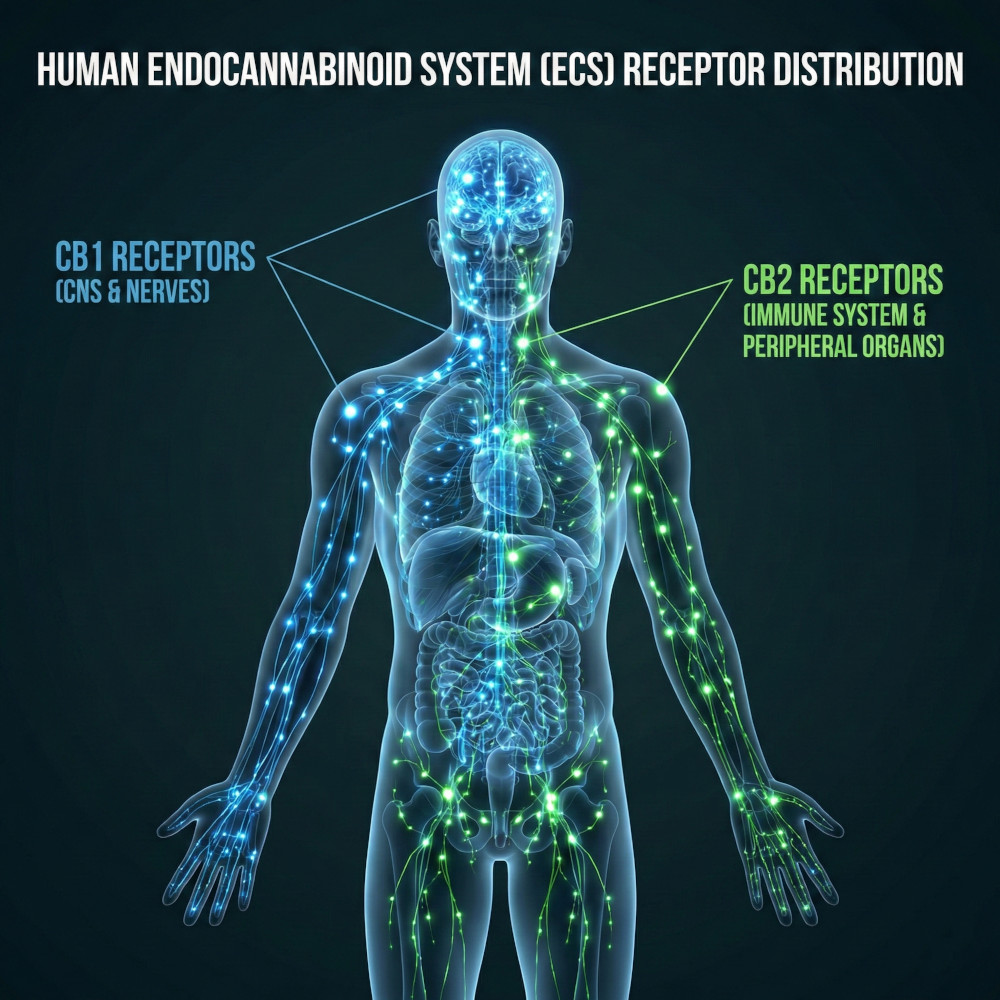 Les récepteurs CB1 (bleu) prédominent dans le cerveau et le système nerveux central, tandis que les récepteurs CB2 (vert) sont plus dispersés, avec une présence accrue dans le système immunitaire et les tissus périphériques.
Les récepteurs CB1 (bleu) prédominent dans le cerveau et le système nerveux central, tandis que les récepteurs CB2 (vert) sont plus dispersés, avec une présence accrue dans le système immunitaire et les tissus périphériques.
Les récepteurs CB2 sont localisés principalement dans les cellules du système immunitaire et dans les tissus périphériques. Leur activation est associée à la modulation de la réponse immunitaire et des processus inflammatoires et de protection tissulaire, sans profil intoxicant typique.
Enfin, les enzymes qui dégradent les endocannabinoïdes — comme la FAAH (associée à l'anandamide) et la MAGL (associée au 2-AG) — aident à réguler le "tonus" endocannabinoïde. Cette composante enzymatique est clé pour comprendre que le SEC ne dépend pas seulement des récepteurs, mais aussi de la durée pendant laquelle les signaux endogènes persistent dans chaque tissu.
Les phytocannabinoïdes du cannabis
Où et comment sont produits les cannabinoïdes de la plante
 La plus grande concentration de phytocannabinoïdes (comme le THC ou le CBD) se trouve à l'intérieur des têtes sphériques des trichomes.
La plus grande concentration de phytocannabinoïdes (comme le THC ou le CBD) se trouve à l'intérieur des têtes sphériques des trichomes.
Les phytocannabinoïdes sont synthétisés principalement dans les trichomes glandulaires, des structures spécialisées qui recouvrent surtout les fleurs et les feuilles proches. Ces glandes sécrétrices produisent une résine riche en cannabinoïdes, terpènes (responsables de l'arôme et du goût) et flavonoïdes, et agissent également comme une interface chimique avec l'environnement (par exemple, face au rayonnement, à la dessiccation ou aux herbivores), ce qui aide à comprendre pourquoi leur abondance et leur composition varient selon la génétique et les conditions de culture.
D'un point de vue biosynthétique, la plupart des cannabinoïdes dérivent d'un précurseur commun : l'acide cannabigérolique (CBGA). Par des voies enzymatiques spécifiques, le CBGA se transforme en THCA, CBDA ou CBCA, en fonction de l'expression génétique de la plante ; c'est pourquoi on parle de chimiotypes (plantes à dominance THC, dominance CBD ou profils mixtes), plus informatifs que les étiquettes commerciales traditionnelles lorsque l'on cherche à prédire l'effet.
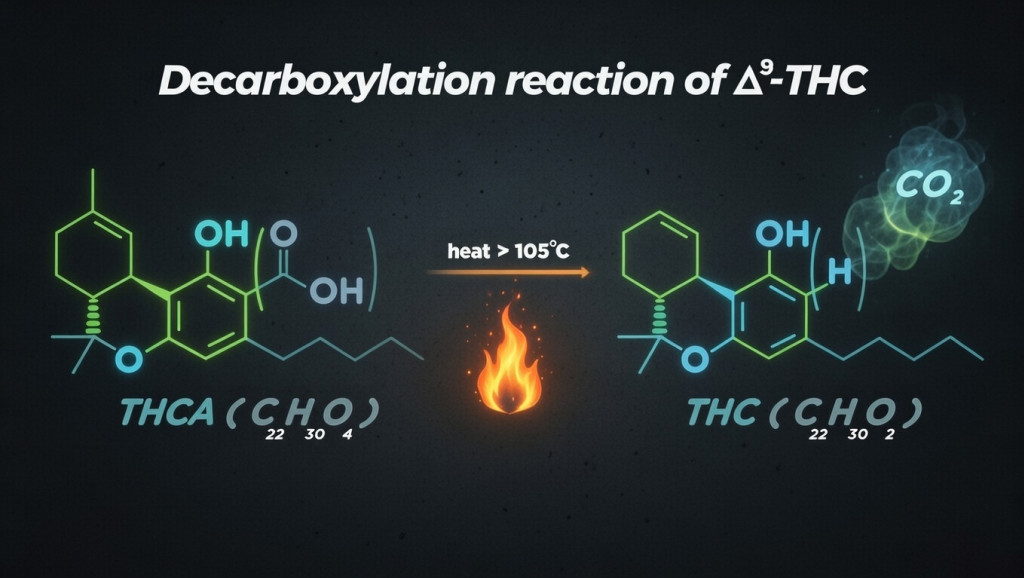
Dans la plante fraîche, les formes acides comme le THCA ou le CBDA prédominent, lesquelles ne produisent pas le profil intoxicant caractéristique du THC. L'application de chaleur déclenche la décarboxylation, transformant ces acides en leurs formes neutres (par exemple, THCA→THC et CBDA→CBD), ce qui change de manière décisive leur effet pharmacologique. Ce détail est clé pour interpréter les différences entre la fleur brute, les extractions non activées et les produits soumis à la chaleur : le "potentiel" d'un matériel ne dépend pas seulement du pourcentage total, mais de la quantité qui est déjà sous forme neutre et de la façon dont il est préparé et consommé.
Si vous voulez comprendre pourquoi la chaleur transforme le THCA en THC et comment cela affecte l'effet final, cet article vous intéressera :
La décarboxylation transforme les cannabinoïdes acides (THCA, CBDA) en formes actives par la chaleur. Des températures de 110-115°C pendant 40-45 minutes optimisent la conversion tout en préservant...
Les cannabinoïdes majeurs de la marijuana
Le THC (delta-9-tétrahydrocannabinol) est le principal phytocannabinoïde intoxicant du cannabis. Son action en tant qu'agoniste partiel des récepteurs CB1, fortement exprimés dans le système nerveux central, explique une bonne partie de ses effets : changements dans la perception sensorielle et du temps, modulation de l'humeur, augmentation de l'appétit et altérations transitoires de fonctions comme l'attention, la mémoire de travail et la coordination motrice. L'intensité et le profil de l'effet dépendent de variables telles que la dose, la voie d'administration (inhalée ou orale), la tolérance et la présence d'autres composés du cannabis pouvant moduler la réponse.
Le CBD (cannabidiol) présente un profil pharmacologique distinct. Il n'est pas intoxicant et n'agit pas comme un agoniste classique du CB1 ; son influence sur le système endocannabinoïde est plus indirecte et "régulatrice", modulant le tonus du système à travers différentes cibles (y compris des enzymes et des récepteurs non exclusivement cannabinoïdes). En termes pratiques, cela aide à comprendre pourquoi le CBD ne produit pas l'effet "high" typique du THC et pourquoi, chez certaines personnes et dans certaines formulations, il peut atténuer certains effets indésirables du THC (comme la nervosité ou la sensation de perte de contrôle), bien que ce résultat ne soit pas automatique et dépende des proportions et des doses réelles.
Les cannabinoïdes mineurs et leur pertinence émergente
Le CBG (cannabigérol) occupe une position spéciale car, sous sa forme acide (CBGA), il est le point de départ biosynthétique à partir duquel la plante génère d'autres familles (THCA, CBDA, CBCA). En termes pharmacologiques, le CBG n'est pas intoxicant au sens classique du THC et est étudié pour son rôle possible en tant que modulateur dans des processus tels que l'inflammation et la douleur, outre son intérêt pour des activités antibactériennes et neuroprotectrices décrites dans la recherche préclinique. Sa relation avec des paramètres oculaires a également été explorée, bien qu'il convienne de formuler cela comme un domaine de recherche plutôt que comme un effet établi chez l'homme.
Le CBN (cannabinol) n'est généralement pas un cannabinoïde "dominant" dans la plante fraîche : il apparaît surtout lorsque le THC se dégrade par vieillissement et oxydation, raison pour laquelle sa présence peut augmenter dans un matériel mal conservé ou très affiné. Il est fréquemment associé à un profil plus sédatif, mais cette idée nécessite des nuances : dans les produits réels, la sensation de somnolence peut dépendre autant du contexte (dose totale, tolérance, moment de la journée) que du reste de l'extrait (autres cannabinoïdes et terpènes).
Le CBN n'est pas un cannabinoïde que la plante produit : il se forme lorsque le THC s'oxyde. Pendant des décennies, cela en a fait un synonyme de cannabis dégradé. On le comprend désormais autreme...
Le THCV (tétrahydrocannabivarine) est l'un des cannabinoïdes "variniques" les plus intéressants pour sa pharmacologie dose-dépendante. À faibles doses, il peut se comporter comme un modulateur ou un antagoniste fonctionnel du CB1 dans certains modèles, tandis qu'à des doses plus élevées, il peut montrer des effets plus proches d'une activation cannabinoïde. Dans la pratique de la vulgarisation, cela se traduit par le fait qu'il est étudié pour sa relation possible avec l'appétit et le métabolisme et, au niveau subjectif, certaines personnes décrivent des effets plus "clairs" ou moins sédatifs que ceux du THC, bien que ces expériences ne soient pas uniformes et dépendent du chimiotype et de la formulation.
Le CBC (cannabichromène) est un cannabinoïde non intoxicant qui apparaît généralement en concentrations plus faibles, mais qui a gagné en intérêt pour son rôle possible dans la modulation de la douleur et de l'inflammation. Son action semble impliquer, au moins en partie, des cibles différentes de CB1/CB2 (par exemple, des canaux impliqués dans la signalisation sensorielle), ce qui en fait un candidat "modulateur" au sein de formulations à large spectre. Sur le plan appliqué, le CBC et le THCV (avec le CBG et d'autres mineurs) impulsent une étape de sélection génétique orientée vers des profils chimiques plus spécifiques, au-delà du binôme THC/CBD.
 Résumé des familles chimiques les plus pertinentes (comme le THC, le CBD et leurs formes acides) et les propriétés thérapeutiques qui leur sont attribuées dans la recherche actuelle.
Résumé des familles chimiques les plus pertinentes (comme le THC, le CBD et leurs formes acides) et les propriétés thérapeutiques qui leur sont attribuées dans la recherche actuelle.
L'effet d'entourage
L'effet dit d'entourage (ou entourage effect) est une hypothèse pharmacologique : elle postule que les effets du cannabis ne dépendent pas seulement du THC ou du CBD séparément, mais de l'ensemble des composés présents dans une préparation (phytocannabinoïdes, terpènes et autres composants minoritaires). Cette idée est utilisée pour expliquer pourquoi deux produits avec un pourcentage de THC similaire peuvent générer des expériences différentes, et pourquoi certains extraits à spectre complet sont perçus comme plus "ronds" que les isolats.
Néanmoins, il convient de nuancer le langage : il ne s'agit pas toujours d'une "synergie" garantie. En pratique, les interactions entre composés peuvent être synergiques, additives ou même antagonistes, et leur expression dépend de variables telles que la dose, les proportions relatives, la voie d'administration, la tolérance et les différences individuelles.
D'un point de vue utile pour le lecteur, l'effet d'entourage invite à regarder au-delà d'un chiffre unique (par exemple, "% de THC"). Dans le domaine thérapeutique et dans le développement de variétés ou d'extraits, il suggère que la reproductibilité du profil chimique complet peut importer autant que la puissance, mais sans en faire un argument commercial : la composition vérifiable, la stabilité et un dosage constant restent la base pour parler avec rigueur.
Dans l'article suivant, nous vous expliquons l'effet d'entourage en profondeur :
Découvrez ce qu'est l'effet d'entourage du cannabis : comment les cannabinoïdes, les terpènes et les flavonoïdes agissent ensemble pour renforcer les effets thérapeutiques.
Les cannabinoïdes font partie d'un système de signalisation profondément intégré dans la physiologie humaine. Le système endocannabinoïde agit comme un axe régulateur fondamental qui relie le système nerveux, le système immunitaire et le métabolisme.
Le cannabis est pertinent parce qu'il produit des phytocannabinoïdes capables d'interagir efficacement avec ce système, et non parce qu'il en est à l'origine. Comprendre cette interaction d'un point de vue scientifique permet d'aborder l'étude du cannabis et de ses composés avec rigueur, en s'éloignant des approches simplistes.
Sources et références
- Lu, H.-C., & Mackie, K. (2021). Review of the Endocannabinoid System. Biological Psychiatry: Cognitive Neuroscience and Neuroimaging, 6(6), 607–615. https://doi.org/10.1016/j.bpsc.2020.07.016 (PMC)[1][2]
- De Petrocellis, L., Cascio, M. G., & Di Marzo, V. (2004). The endocannabinoid system: a general view and latest additions. British Journal of Pharmacology, 141(5), 765–774. https://doi.org/10.1038/sj.bjp.0705666 (PMC)[3][4]
- Di Marzo, V., Bifulco, M., & De Petrocellis, L. (2004). The endocannabinoid system and its therapeutic exploitation. Nature Reviews Drug Discovery, 3(9), 771–784. <https://doi.org/10.1038/nrd1495>[5]
- Devane, W. A., Hanus, L., Breuer, A., et al. (1992). Isolation and structure of a brain constituent that binds to the cannabinoid receptor. Science. (Article classique : anandamide/AEA). PubMed: 1470919[6]
- Russo, E. B. (2011). Taming THC: potential cannabis synergy and phytocannabinoid-terpenoid entourage effects. British Journal of Pharmacology, 163(7), 1344–1364. https://doi.org/10.1111/j.1476-5381.2011.01238.x (PMC)[7][8]
- Gertsch, J., Leonti, M., Raduner, S., et al. (2008). Beta-caryophyllene is a dietary cannabinoid. Proceedings of the National Academy of Sciences of the United States of America (PNAS). <https://doi.org/10.1073/pnas.0803601105>[9][10]
- Long, J. Z., Li, W., Booker, L., et al. (2009). Dual blockade of FAAH and MAGL identifies behavioral processes regulated by endocannabinoid crosstalk in vivo. PNAS. <https://doi.org/10.1073/pnas.0909411106>[11]
- Targeting Endocannabinoid Signaling: FAAH and MAG Lipase… (2021). Annual Review of Pharmacology and Toxicology. <https://doi.org/10.1146/annurev-pharmtox-030220-112741>[12]
- Wang, M., Wang, Y.-H., Avula, B., et al. (2016). Decarboxylation Study of Acidic Cannabinoids: A Novel Approach Using Ultra-High-Performance Supercritical Fluid Chromatography/Photodiode Array-Mass Spectrometry. Cannabis and Cannabinoid Research, 1(1), 262–271. https://doi.org/10.1089/can.2016.0020 (PMC)[13][14]
- Castaneto, M. S., Gorelick, D. A., Desrosiers, N. A., et al. (2014). Synthetic Cannabinoids: Pharmacology, Behavioral Effects, and Abuse Potential. (Revue ; utile pour différencier THC vs synthétiques à haute efficacité). https://doi.org/10.1097/FBP.0000000000000034 (PMC)[15]