¿Qué son los cannabinoides?
Los cannabinoides son compuestos orgánicos de naturaleza lipídica, capaces de modular un sistema de señalización del organismo humano: el sistema endocannabinoide (SEC). Este sistema participa en la regulación de procesos como la neurotransmisión, la respuesta inmunitaria y la inflamación, el metabolismo energético, la nocicepción (percepción del dolor) y la respuesta al estrés.
El mecanismo de acción de los cannabinoides se basa en su capacidad para unirse a receptores concretos distribuidos por distintos tejidos. Esta interacción puede activar o inhibir cascadas de señalización intracelular, alterando la liberación de neurotransmisores, la expresión génica o la respuesta inflamatoria. La especificidad del efecto depende tanto del tipo de cannabinoide como del receptor implicado y del contexto fisiológico en el que se produce la señal.
Aunque el término cannabinoide se asocia de inmediato al cannabis, su significado es más amplio. Existen cannabinoides producidos por el propio organismo, compuestos de origen vegetal y moléculas sintetizadas en laboratorio, todos ellos capaces de modular principalmente el SEC (y, en algunos casos, otras vías de señalización relacionadas).
Tipos de cannabinoides y compuestos que modulan el sistema endocannabinoide
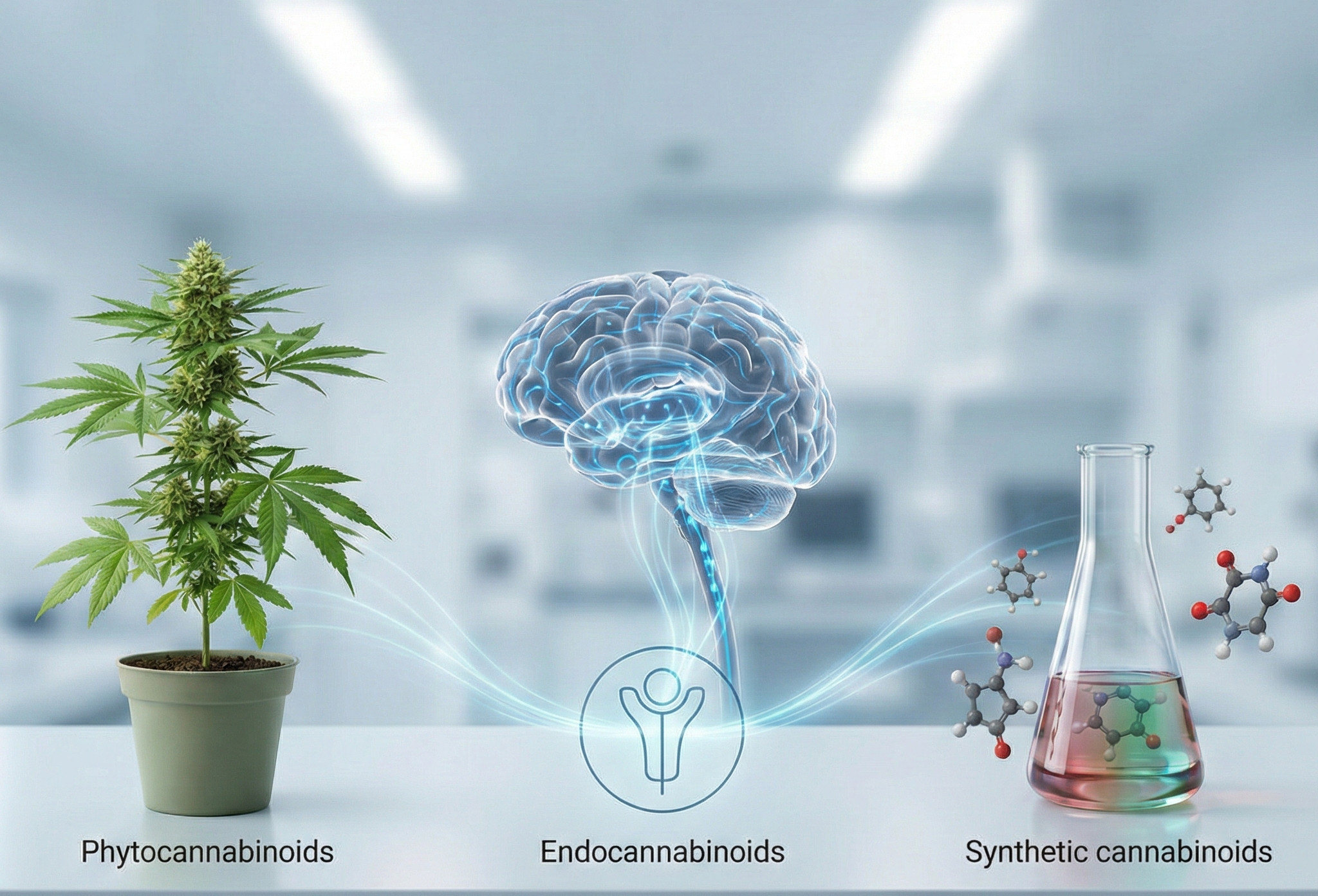 Aunque interactúan con los mismos receptores, el origen de estos compuestos varía drásticamente: desde la biosíntesis natural en la planta o el cerebro, hasta el origen sintético
Aunque interactúan con los mismos receptores, el origen de estos compuestos varía drásticamente: desde la biosíntesis natural en la planta o el cerebro, hasta el origen sintético
Endocannabinoides: los que produce el organismo
Los endocannabinoides son cannabinoides sintetizados de manera endógena por el cuerpo humano y otros mamíferos. No se almacenan en grandes cantidades, sino que se producen bajo demanda a partir de precursores lipídicos presentes en las membranas celulares.
Los dos principales endocannabinoides caracterizados son la anandamida (AEA) y el 2-araquidonoilglicerol (2-AG). Ambos participan activamente en la modulación de la neurotransmisión, la respuesta al estrés, el apetito, la memoria y los procesos inflamatorios. A diferencia de muchos neurotransmisores clásicos, los endocannabinoides actúan de forma retrógrada, regulando la liberación de otros mensajeros químicos.
Se ha descrito la presencia de endocannabinoides en la leche materna y se ha propuesto que podrían participar en conductas tempranas como la succión y en aspectos del desarrollo; no obstante, el detalle de esos mecanismos en humanos sigue siendo un área activa de investigación.
Fitocannabinoides: los de origen vegetal
Los fitocannabinoides son cannabinoides sintetizados por plantas, siendo Cannabis sativa L. una de las fuentes más ricas y diversas conocida hasta la fecha. Aunque se han identificado compuestos con actividad cannabimimética en otras especies vegetales, el cannabis destaca por la cantidad, variedad y potencia de los fitocannabinoides que produce.
Durante décadas se asumió que estos compuestos eran exclusivos del cannabis. Si bien hoy se sabe que no es estrictamente cierto, esta planta sigue siendo la de mayor relevancia farmacológica y biológica en relación con el sistema endocannabinoide, motivo por el cual constituye el foco principal del análisis en este ámbito.
Cannabinoides sintéticos: moléculas diseñadas en laboratorio
Los cannabinoides sintéticos son compuestos creados artificialmente con el objetivo de interactuar con los receptores cannabinoides. Algunos de ellos han sido desarrollados con fines terapéuticos, como el dronabinol, utilizado en contextos clínicos específicos bajo supervisión médica.
Debe distinguirse entre cannabinoides sintéticos empleados como fármacos (por ejemplo, dronabinol en contextos clínicos concretos) y las mezclas recreativas tipo K2/Spice. En estas últimas, la composición suele ser incierta y algunos compuestos pueden activar CB1 de manera intensa (incluso como agonistas completos), lo que se asocia a un perfil de efectos adversos y toxicidad más impredecible que el del THC.
Cannabinoides miméticos o cannabimiméticos
Existen compuestos que, sin pertenecer químicamente a la familia de los cannabinoides, imitan su acción o modulan el sistema endocannabinoide. Estos se encuentran en diversas plantas y alimentos.
El beta-cariofileno, presente en la pimienta negra, el clavo y el cannabis, es uno de los ejemplos más estudiados por su afinidad selectiva por los receptores CB2. Otros compuestos presentes en la equinácea, el cacao o determinadas trufas también interactúan indirectamente con este sistema, lo que refuerza su papel como interfaz bioquímica entre dieta, entorno y fisiología humana.
El sistema endocannabinoide (SEC)
El sistema endocannabinoide (SEC) es una red reguladora compleja compuesta por receptores cannabinoides, endocannabinoides (mensajeros lipídicos producidos por el organismo) y enzimas responsables de su síntesis y degradación. En conjunto, contribuye a la homeostasis, ajustando múltiples procesos fisiológicos ante cambios internos o externos.
Una característica distintiva del SEC es que muchos endocannabinoides se sintetizan "bajo demanda" a partir de lípidos de membrana y actúan localmente durante poco tiempo. En el sistema nervioso pueden funcionar como señales retrógradas: la neurona postsináptica libera endocannabinoides que actúan sobre terminales presinápticas, modulando la liberación de neurotransmisores y la plasticidad sináptica.
Los receptores CB1 se expresan de forma predominante en el sistema nervioso central, especialmente en regiones implicadas en cognición, memoria, control motor y percepción del dolor. Su activación explica buena parte de los efectos neurológicos del THC, ya que modifica la señalización sináptica y el equilibrio de circuitos neuronales implicados en esas funciones.
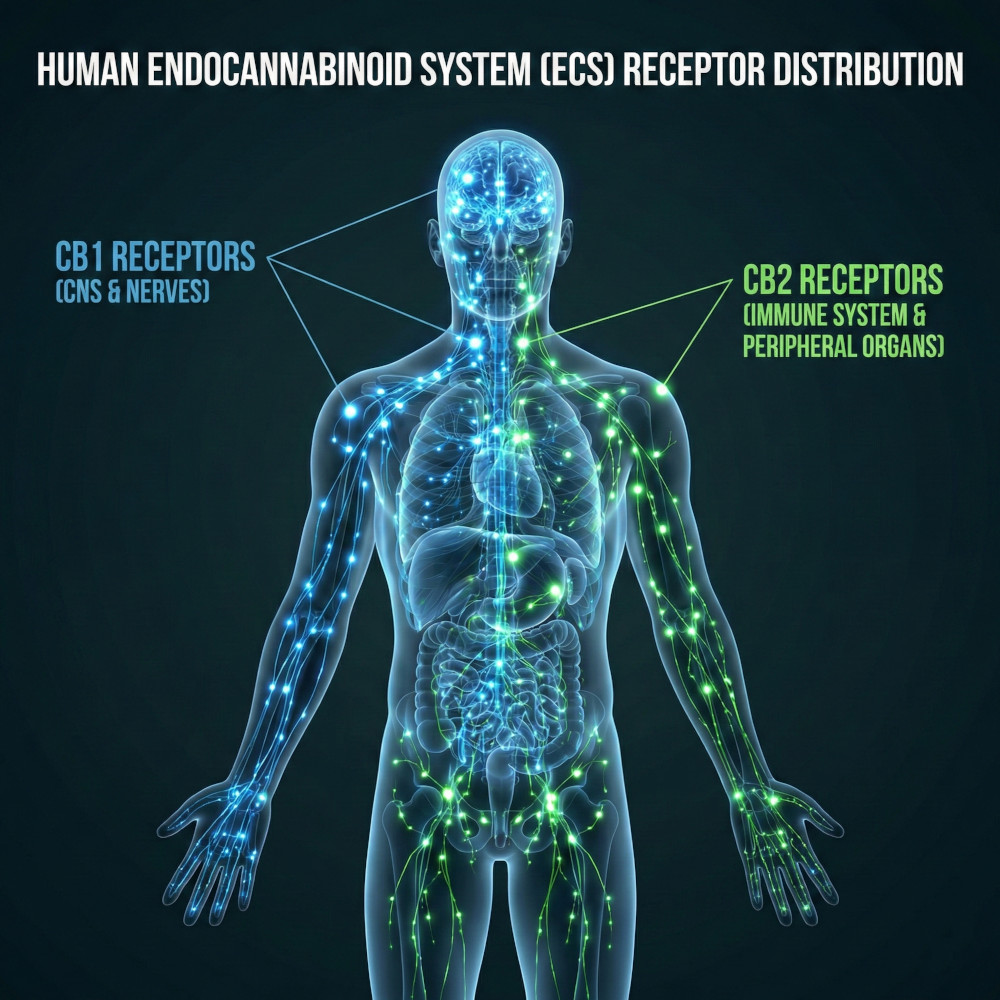 Los receptores CB1 (azul) predominan en el cerebro y el sistema nervioso central, mientras que los CB2 (verde) se encuentran más dispersos, con mayor presencia en el sistema inmunitario y tejidos periféricos.
Los receptores CB1 (azul) predominan en el cerebro y el sistema nervioso central, mientras que los CB2 (verde) se encuentran más dispersos, con mayor presencia en el sistema inmunitario y tejidos periféricos.
Los receptores CB2 se localizan principalmente en células del sistema inmunitario y en tejidos periféricos. Su activación se asocia a la modulación de la respuesta inmune y de procesos inflamatorios y de protección tisular, sin un perfil intoxicante típico.
Por último, las enzimas que degradan endocannabinoides —como FAAH (asociada a anandamida) y MAGL (asociada a 2-AG)— ayudan a regular el "tono" endocannabinoide. Este componente enzimático es clave para entender que el SEC no solo depende de receptores, sino también de cuánto tiempo persisten las señales endógenas en cada tejido.
Los fitocannabinoides del cannabis
Dónde y cómo se producen los cannabinoides de la planta
 La mayor concentración de fitocannabinoides (como el THC o el CBD) se encuentra dentro de las cabezas esféricas de los tricomas
La mayor concentración de fitocannabinoides (como el THC o el CBD) se encuentra dentro de las cabezas esféricas de los tricomas
Los fitocannabinoides se sintetizan principalmente en los tricomas glandulares, estructuras especializadas que recubren sobre todo las flores y las hojas cercanas. Estas glándulas secretoras producen una resina rica en cannabinoides, terpenos (responsables del aroma y sabor) y flavonoides, y actúan también como una interfaz química con el entorno (por ejemplo, frente a radiación, desecación o herbivoría), lo que ayuda a entender por qué su abundancia y composición varían según genética y condiciones de cultivo.
Desde el punto de vista biosintético, la mayoría de los cannabinoides derivan de un precursor común: el ácido cannabigerólico (CBGA). Mediante rutas enzimáticas específicas, el CBGA se transforma en THCA, CBDA o CBCA, en función de la expresión genética de la planta; por eso se habla de quimiotipos (plantas con dominancia THC, dominancia CBD o perfiles mixtos), más informativos que etiquetas comerciales tradicionales cuando lo que se busca es predecir el efecto.
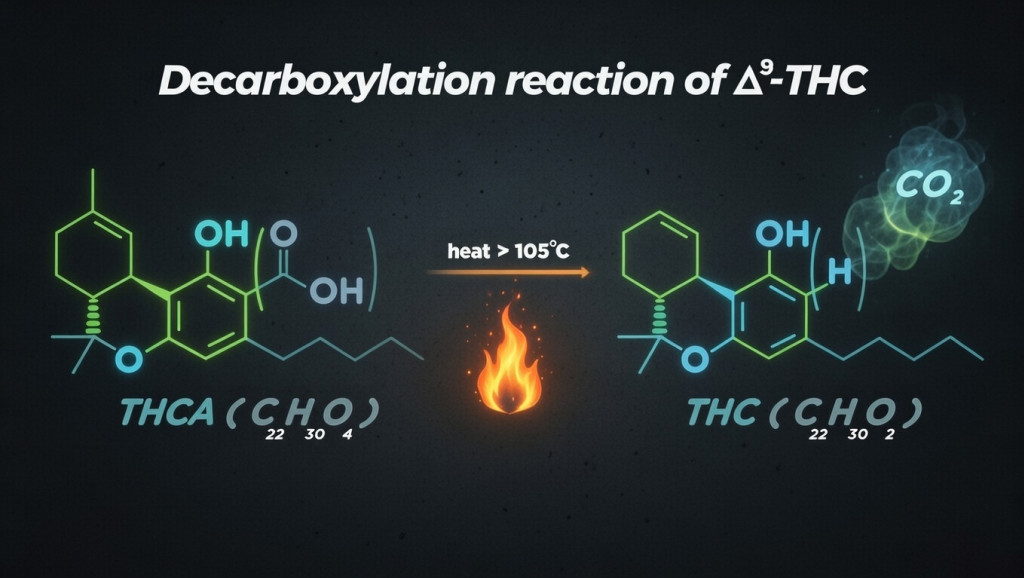
En la planta fresca, predominan formas ácidas como THCA o CBDA, que no producen el perfil intoxicante característico del THC. La aplicación de calor desencadena la descarboxilación, transformando esos ácidos en sus formas neutras (por ejemplo, THCA→THC y CBDA→CBD), lo que cambia de manera decisiva su efecto farmacológico. Este detalle es clave para interpretar diferencias entre flor cruda, extracciones sin activar y productos sometidos a calor: el “potencial” de un material no depende solo del porcentaje total, sino de cuánto está ya en forma neutra y de cómo se prepara y consume.
Si quieres entender por qué el calor transforma THCA en THC y cómo afecta al efecto final, te interesará este artículo:
La descarboxilación transforma los cannabinoides ácidos (THCA, CBDA) en sus formas activas mediante calor. Temperaturas de 110-115°C durante 40-45 minutos optimizan la conversión preservando terpen...
Los cannabinoides mayores de la marihuana
El THC (delta-9-tetrahidrocannabinol) es el principal fitocannabinoide intoxicante del cannabis. Su acción como agonista parcial de los receptores CB1, altamente expresados en el sistema nervioso central, explica buena parte de sus efectos: cambios en la percepción sensorial y del tiempo, modulación del estado de ánimo, aumento del apetito y alteraciones transitorias de funciones como la atención, la memoria de trabajo y la coordinación motora. La intensidad y el perfil del efecto dependen de variables como la dosis, la vía de administración (inhalada u oral), la tolerancia y la presencia de otros compuestos del cannabis que puedan modular la respuesta.
El CBD (cannabidiol) presenta un perfil farmacológico distinto. No es intoxicante y no actúa como un agonista clásico de CB1; su influencia sobre el sistema endocannabinoide es más indirecta y “reguladora”, modulando el tono del sistema a través de distintas dianas (incluidas enzimas y receptores no exclusivamente cannabinoides). En términos prácticos, esto ayuda a entender por qué el CBD no produce el “colocón” típico del THC y por qué, en algunas personas y formulaciones, puede suavizar ciertos efectos indeseables del THC (como nerviosismo o sensación de descontrol), aunque ese resultado no es automático y depende de proporciones y dosis reales.
Los cannabinoides menores y su relevancia emergente
El CBG (cannabigerol) ocupa una posición especial porque, en su forma ácida (CBGA), es el punto de partida biosintético a partir del cual la planta genera otras familias (THCA, CBDA, CBCA). En términos farmacológicos, el CBG no es intoxicante en el sentido clásico del THC y se estudia por su posible papel como modulador en procesos como inflamación y dolor, además de su interés por actividades antibacterianas y neuroprotectoras descritas en investigación preclínica. También se ha explorado su relación con parámetros oculares, aunque conviene formularlo como un campo en investigación más que como un efecto establecido en humanos.
El CBN (cannabinol) no suele ser un cannabinoide "dominante" en la planta fresca: aparece sobre todo cuando el THC se degrada por envejecimiento y oxidación, motivo por el cual su presencia puede aumentar en material mal conservado o muy curado. Se asocia con frecuencia a un perfil más sedante, pero esta idea requiere matices: en productos reales, la sensación de somnolencia puede depender tanto del contexto (dosis total, tolerancia, hora del día) como del resto del extracto (otros cannabinoides y terpenos).
El CBN no es un cannabinoide que la planta produzca: se forma cuando el THC se oxida. Durante décadas eso lo convirtió en sinónimo de cannabis degradado. Ahora se entiende como algo distinto: un pe...
El THCV (tetrahidrocannabivarina) es uno de los cannabinoides “varínicos” más interesantes por su farmacología dependiente de dosis. A dosis bajas puede comportarse como modulador o antagonista funcional de CB1 en ciertos modelos, mientras que a dosis más altas puede mostrar efectos más cercanos a una activación cannabinoide. En la práctica divulgativa, esto se traduce en que se investiga por su posible relación con apetito y metabolismo y, a nivel subjetivo, algunas personas describen efectos más “claros” o menos sedantes que los del THC, aunque estas experiencias no son uniformes y dependen del quimiotipo y de la formulación.
El CBC (cannabicromeno) es un cannabinoide no intoxicante que suele aparecer en concentraciones menores, pero que ha ganado interés por su posible papel en la modulación de dolor e inflamación. Su acción parece involucrar, al menos en parte, dianas distintas de CB1/CB2 (por ejemplo, canales implicados en señalización sensorial), lo que lo convierte en un candidato a “modulador” dentro de formulaciones de espectro amplio. En el plano aplicado, CBC y THCV (junto con CBG y otros menores) están impulsando una etapa de selección genética orientada a perfiles químicos más específicos, más allá del binomio THC/CBD.
 Resumen de las familias químicas más relevantes (como THC, CBD y sus formas ácidas) y las propiedades terapéuticas que se les atribuyen en la investigación actual.
Resumen de las familias químicas más relevantes (como THC, CBD y sus formas ácidas) y las propiedades terapéuticas que se les atribuyen en la investigación actual.
El efecto séquito
El llamado efecto séquito (o entourage effect) es una hipótesis farmacológica: plantea que los efectos del cannabis no dependen solo del THC o del CBD por separado, sino del conjunto de compuestos presentes en una preparación (fitocannabinoides, terpenos y otros componentes minoritarios). Esta idea se utiliza para explicar por qué dos productos con un porcentaje de THC similar pueden generar experiencias distintas, y por qué algunos extractos de espectro completo se perciben como más “redondos” que los aislados.
Aun así, conviene matizar el lenguaje: no siempre se trata de una “sinergia” garantizada. En la práctica, las interacciones entre compuestos pueden ser sinérgicas, aditivas o incluso antagonistas, y su expresión depende de variables como dosis, proporciones relativas, vía de administración, tolerancia y diferencias individuales.
Desde un punto de vista útil para el lector, el efecto séquito invita a mirar más allá de un único número (por ejemplo, “% de THC”). En el ámbito terapéutico y en el desarrollo de variedades o extractos, sugiere que la reproducibilidad del perfil químico completo puede importar tanto como la potencia, pero sin convertirlo en un argumento comercial: la composición verificable, la estabilidad y una dosificación consistente siguen siendo la base para hablar con rigor.
En el siguiente artículo, te explicamos el efecto séquito en profundidad:
Descubre qué es el efecto séquito del cannabis: cómo cannabinoides, terpenos y flavonoides trabajan juntos para potenciar efectos terapéuticos.
Los cannabinoides forman parte de un sistema de señalización profundamente integrado en la fisiología humana. El sistema endocannabinoide actúa como un eje regulador fundamental que conecta el sistema nervioso, el sistema inmunitario y el metabolismo.
El cannabis resulta relevante porque produce fitocannabinoides capaces de interactuar eficazmente con este sistema, no porque lo origine. Comprender esta interacción desde una perspectiva científica permite abordar el estudio del cannabis y sus compuestos con rigor, alejándose de enfoques simplistas.
Fuentes y referencias
- Lu, H.-C., & Mackie, K. (2021). Review of the Endocannabinoid System. Biological Psychiatry: Cognitive Neuroscience and Neuroimaging, 6(6), 607–615. https://doi.org/10.1016/j.bpsc.2020.07.016 (PMC)[1][2]
- De Petrocellis, L., Cascio, M. G., & Di Marzo, V. (2004). The endocannabinoid system: a general view and latest additions. British Journal of Pharmacology, 141(5), 765–774. https://doi.org/10.1038/sj.bjp.0705666 (PMC)[3][4]
- Di Marzo, V., Bifulco, M., & De Petrocellis, L. (2004). The endocannabinoid system and its therapeutic exploitation. Nature Reviews Drug Discovery, 3(9), 771–784. <https://doi.org/10.1038/nrd1495>[5]
- Devane, W. A., Hanus, L., Breuer, A., et al. (1992). Isolation and structure of a brain constituent that binds to the cannabinoid receptor. Science. (Artículo clásico: anandamida/AEA). PubMed: 1470919[6]
- Russo, E. B. (2011). Taming THC: potential cannabis synergy and phytocannabinoid-terpenoid entourage effects. British Journal of Pharmacology, 163(7), 1344–1364. https://doi.org/10.1111/j.1476-5381.2011.01238.x (PMC)[7][8]
- Gertsch, J., Leonti, M., Raduner, S., et al. (2008). Beta-caryophyllene is a dietary cannabinoid. Proceedings of the National Academy of Sciences of the United States of America (PNAS). <https://doi.org/10.1073/pnas.0803601105>[9][10]
- Long, J. Z., Li, W., Booker, L., et al. (2009). Dual blockade of FAAH and MAGL identifies behavioral processes regulated by endocannabinoid crosstalk in vivo. PNAS. <https://doi.org/10.1073/pnas.0909411106>[11]
- Targeting Endocannabinoid Signaling: FAAH and MAG Lipase… (2021). Annual Review of Pharmacology and Toxicology. <https://doi.org/10.1146/annurev-pharmtox-030220-112741>[12]
- Wang, M., Wang, Y.-H., Avula, B., et al. (2016). Decarboxylation Study of Acidic Cannabinoids: A Novel Approach Using Ultra-High-Performance Supercritical Fluid Chromatography/Photodiode Array-Mass Spectrometry. Cannabis and Cannabinoid Research, 1(1), 262–271. https://doi.org/10.1089/can.2016.0020 (PMC)[13][14]
- Castaneto, M. S., Gorelick, D. A., Desrosiers, N. A., et al. (2014). Synthetic Cannabinoids: Pharmacology, Behavioral Effects, and Abuse Potential. (Revisión; útil para diferenciar THC vs sintéticos de alta eficacia). https://doi.org/10.1097/FBP.0000000000000034 (PMC)[15]